როგორ შეიქმნა კოვიდ-19-ის ვაქცინა ასე სწრაფად?
და რატომაა ის უსაფრთხო?
ადრე ვაქცინის შექმნას ხანდახან 15 წელიც კი სჭირდებოდა. მაშ, როგორ მოახერხეს მეცნიერებმა ვაქცინის შექმნა 7-8 თვეში?
ვაქცინის შექმნის და წარმოების პროცესი ბევრი საფეხურისგან შედგება.
მაგრამ სანამ ამ პროცესს განვიხილავთ, მოდით, განვმარტოთ ერთი-ორი ტერმინი, რომ ყველაფერი უფრო გასაგები იყოს.
რა არის პათოგენი?
პათოგენი არის ინფექციური დაავადების გამომწვევი. კოვიდ-19-ის შემთხვევაში - ვირუსი.
რა არის იმუნური სისტემა?
ჩვენი ორგანიზმის ძალიან გამართული სისტემა, რომელიც ბევრი უჯრედისგან შედგება და 24/7-ზე ზრუნავს ჩვენს ჯანმრთელობაზე.
რა არის ანტიგენი?
ჩვენს იმუნურ სისტემას ვირუსის, როგორც ერთი მთლიანობის, დანახვა არ შეუძლია. მისი გააქტიურებისთვის და შემდეგ სასრუველი პასუხის გამომუშავებისთვის საჭიროა, სპეციალურმა უჯრედებმა ვირუსები პატარა ნაწილებად - ანტიგენებად დაშალონ. ვაქცინები სწორედ ამ ანტიგენებს შეიცავენ.
რა არის პრე-კლინიკური კვლევები?
სანამ ვაქცინის კვლევის პროცესი ადამიანებზე დაიწყება, საჭიროა, რომ ცდები ცხოველებზე ჩატარდეს. მხოლოდ იმ შემთხვევაში დაიწყება ადამიანებზე კვლევა, თუ პრე-კლინიკურ კვლევებში ვაქცინის უსაფრთხოება და ეფექტურობა დადასტურდება.
რა არის კლინიკური კვლევები?
ვაქცინის კლინიკური კვლევა არის პროცესი, რომლის დროსაც მეცნიერები ცდილობენ, დაადგინონ ეფექტური და, რაც მთავარია, უსაფრთხოა თუ არა მათი ვაქცინა.
კლინიკური კვლევები 3 ფაზისგან შედგება:
I ფაზა - ამ ფაზაში 100-მდე ადამიანია ჩართული და მოწმდება ვაქცინის უსაფრთხოება და ეფექტურობა.
II ფაზა - ამ ფაზაში 300-400 ადამიანია ჩართული და კვლავ მოწმდება ვაქცინის უსაფრთხოება და ეფექტურობა
III ფაზა - ამ ფაზაში რამდენიმე ათასი ადამიანია ჩართული და კიდევ უფრო ფართო მასშტაბებზე მოწმდება ვაქცინის უსაფრთხოება და ეფექტურობა.
IV ფაზა - ამ ფაზაში ვაქცინა უკვე ბაზარზეა და მილიონობით ადამიანი იცრება, თუმცა მარეგულირებელი სააგენტო კომპანიებს ავალდებულებს, რომ დაახლოებით 10 წლის განმავლობაში შეაგროვონ მონაცემები ვაქცინის უსაფრთხოებასა და ეფექტურობაზე.
რას საქმიანობს ეთიკის კომისია?
იმისათვის, რომ მეცნიერებმა პრე-კლინიკური ან კლინიკური კვლევები ჩაატარონ, საჭიროა ეთიკის კომისიის თანხმობა. მათ გარეშე პროცესი წინ ვერ წავა.
რა დანიშნულება აქვს მარეგულირებელ სააგენტოს?
ამერიკის წამლისა და საკვების სააგენტო (FDA) და ევროპის მედიცინის სააგენტო (EMA) განიხილავენ ნებისმიერი იმ სამედიცინო პროდუქტის უსაფრთხოებას და ეფექტურობას, რომელმაც კლინიკური კვლევები გაიარა და უკვე მზად არის ბაზარზე გამოსაჩენად. ამ სააგენტოების თანხმობის გარეშე ვერცერთი პროდუქტი ვერ მოხვდება ევროპისა თუ ამერიკის მარკეტზე. მათ არანაირი ფინანსური ინტერესი არ აქვს და მხოლოდ 1 საქმე ემსახურებიან: ადამიანებამდე მიაღწიოს რაც შეიძლება უსაფრთხო და ეფექტურმა პროდუქტმა.
ვაქცინის შექმნის პროცესი
ანტიგენის შერჩევა
ჩვეულებრივ პირობებში შეიძლება, ანტიგენისა და ვაქცინის ტიპის შერჩევას 6-8 წელი დასჭირდეს. ამ შემთხვევაში გაგვიმართლა და წარსული გამოცდილება გამოგვადგა.
2002-2004 და 2012 წლებში აღმოსავლეთ და შუა აზიაში იყო სხვა კორონავირუსების - SARS და MERS ვირუსების - ეპიდემია. ამ ვირუსების საწინააღმდეგო ვაქცინის შექმნაზე მეცნიერებს მუშაობა დაწყებული ჰქონდათ, მაგრამ რადგან პანდემია მალევე ჩაახშეს, ვაქცინის წარმოებას აზრი დაეკარგა.
სამაგიეროდ, მიღებული ცოდნა Covid-19 პანდემიის ჩახშობაში დაგვეხმარა .2019 წელს ჩინეთში კოვიდ-19-ის დაფიქსირებიდან 1 კვირაში მეცნიერებმა უკვე იცოდნენ ვირუსის მთლიანი გენეტიკური მასალა. მეტიც, ჩვენი სხეული ზუსტად იმავე ანტიგენზე აწარმოებდა პასუხს, რაზეც SARS-ისა და MERS-ის შემთხვევაში. მეცნიერებმა რამდენიმე კვირაში უკვე იცოდნენ, რას გამოიყენებდნენ ვაქცინაში ანტიგენად.
6-8 წელი გახდა 1 კვირა.
კლინიკური კვლევები და წარმოება
პრე-კლინიკური და შემდეგ კლინიკური კვლევების დასაწყებად ეთიკის კომისიების თანხმობა გვჭირდება. ჯამში ორივეს 1-1,5 წელიც კი შეიძლება დაჭირდეს. რადგან კოვიდ-19-ის პანდემიამ მთელი მსოფლიო მოიცვა, კომისიებმა ყველა სხვა საქმე გვერდზე გადადეს და მთელი ორგანიზაციული რესურსების მობილიზებით მხოლოდ იმ განაცხადების განხილვა დაიწყეს, რომელიც კოვიდ-19-ის ვაქცინებს თუ სამკურნალო საშუალებებს ეხებოდა. შედეგად, ეს პროცესი სულ რამდენიმე კვირას გაგრძელდა.
კლინიკური კვლევები შეიძლება, 5-6 წელი გაგრძელდეს ორი მიზეზის გამო:
კვლევაში ჩასართავი ადამიანების მოძიებას დიდი დრო სჭირდება;
ასევე ძალიან დიდი ფინანსებია საჭირო.
მაღალი საზოგადოებრივი ინტერესის გამო მსურველიც ბევრი იყო და განვითარებულმა ქვეყნებმაც ძალიან დიდი ფინანსები გამოჰყვეს. შესაბამისად, პროცესი ძალიან დაჩქარდა.
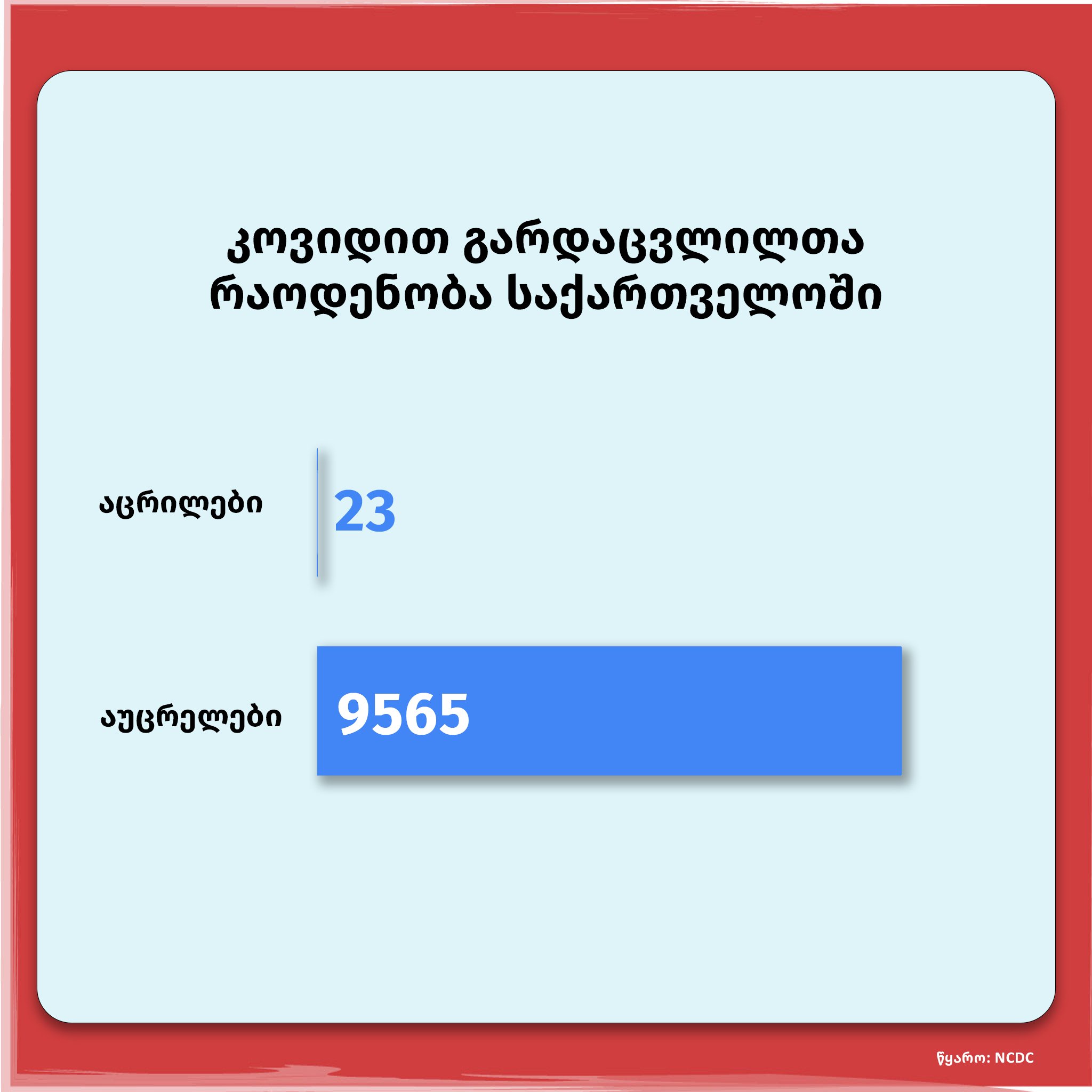
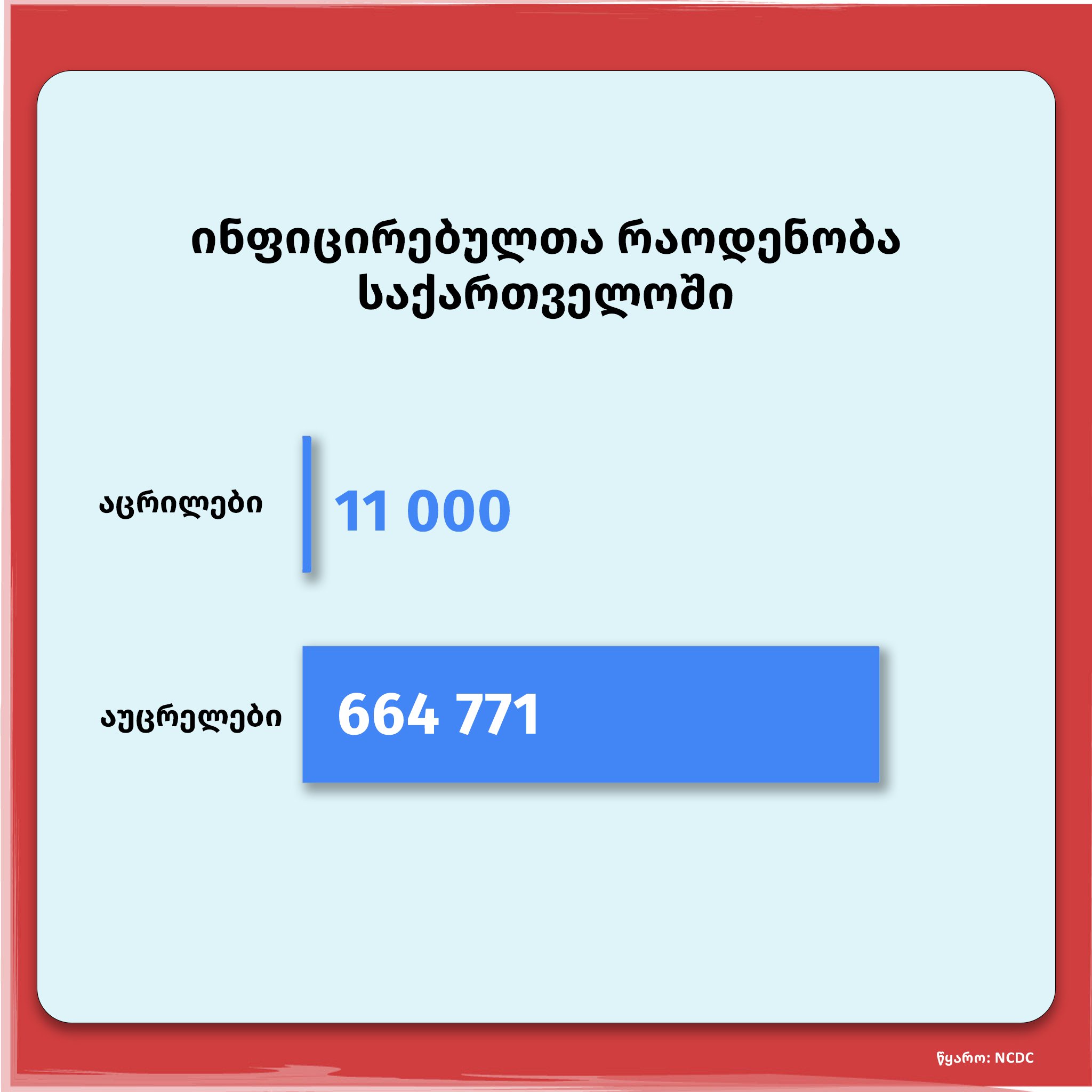
ასევე, კოვიდ-19-მა, როგორც დაავადებამ იმის საშუალება მოგვცა, რომ საცდელი ვაქცინის ეფექტურობა მალევე გვენახა. კვლევაში ჩართული ათასობით აცრილი ადამიანის მონაცემები შეადარეს აუცრელი ადამიანის მონაცემებს და ნახეს, რომ აცრილ ადამიანებში მძიმედ მიმდინარე კოვიდ-19 პრაქტიკულად არ ხვდებოდათ, ამ შედეგის ნახვას კი საშუალოდ 1,5 თვე დასჭირდა თითო ფაზაში. ამასთანავე, პირველი და მეორე ფაზები ერთმანეთის პარალელურად მიმდინარეობდა.
5-6 წელი გახდა 4-6 თვე.
კლინიკური კვლევების პარალელურად კომპანიები დიდ ფინანსურ რისკზე წავიდნენ და წინასწარ დაიწყეს ვაქცინების წარმოება.
მარეგულირებლის თანხმობა
ამის შემდეგ კომპანიებმა ავტორიზაციისთვის მიმართეს მარეგულირებელ სააგენტოებს, რომ ბაზარზე გასვლის უფლება მიეღოთ. ეს პროცესი 1-2 წელი გრძელდება ხოლმე, თუმცა პანდემიის გამო ამ სააგენტოებმაც ყველა საქმე გვერდზე გადადეს და გადაწყვიტეს, რომ მხოლოდ და მხოლოდ კოვიდ-19-თან საბრძოლველი საშუალებები განეხილათ.
1-2 წელი გახდა 3-4 კვირა.
ფარმაცევტული კომპანიებისთვის პროცესი აქ არ სრულდება და ისინი ვალდებულები არიან, გააგრძელონ მონაცემების შეგროვებაზე ვაქცინის უსაფრთხოებასა და ეფექტურობაზე საშუალოდ 10 წლის განმავლობაში. ამას pharmacovigilance-ს ვუწოდებთ.
კოვიდ-19-ის საწინააღმდეგო არსებულ ვაქცინებს არც ერთი ის საფეხური არ გამოუტოვებია, რასაც სხვა, ‘ტრადიციული’ ვაქცინები გადის ხოლმე. მათი უსაფრთხოება და ეფექტურობა იმავე გზითა და ხერხებით დადასტურდა, როგორც ეს ჩვეულებრივ ხდება ხოლმე.
შეკითხვების შემთხვევაში დაგვიკავშირდით ან გამოგვეხმაურეთ Facebook-ზე.